全世界,都在等中國新藥!
今年 7 月,中國醫藥圈被一筆百億美元級交易點燃。
恆瑞醫藥與全球製藥巨頭葛蘭素史克達成 125 億美元 合作,共同開發多達 12 款 創新藥物,創下中國創新藥出海的新紀錄。
而就在此前一個月,中國創新藥 澤立美®(本維莫德乳膏) 亦創造了一項里程碑。
被譽為「全球皮膚科風向標」的美國皮膚病學會(AAD),以史上最快速度——僅 23 個月 完成修訂,打破特應性皮炎治療金標準的修訂紀錄,並將 澤立美®(本維莫德乳膏) 列入最高等級的「強烈推薦」。
這意味著,全球 160 個國家和地區 的皮膚科醫師,首次在權威指南中被明確指引:在治療濕疹時,優先使用中國藥。
從近年的交易熱潮,到澤立美® 的先行探索,中國藥企正持續為全世界提供全新的創新藥物。
打破紀錄
破紀錄了!
2025 年上半年,中國創新藥 License-out(許可授權) 總金額已接近 660 億美元,不僅超過去年全年總額,亦創下中國創新藥出海的新紀錄。
創新藥 BD 交易持續火爆,交易金額不斷刷新高點。
5 月 20 日,三生與輝瑞達成合作,首付款高達 12.5 億美元,總交易金額超過 60 億美元,刷新國產創新藥首付款紀錄。
7 月 28 日,恆瑞醫藥與葛蘭素史克簽署戰略合作協議,將共同開發多達 12 款 創新藥物,首付款 5 億美元,未來潛在投入總金額高達 1,200 億美元。

恆瑞醫藥公告
10 月 22 日,信達生物與武田製藥達成新一代 IO 與 ADC 療法合作,首付款為 12 億美元,合作總金額高達 1,140 億美元。
BD(Business Development,商務拓展)是指醫藥企業透過合作、授權、併購、技術轉讓等方式,實現資源整合、管線補充、市場拓展或風險共擔的商業行為。
其中,創新藥的許可授權,是 BD 最常見的一種形式。
過去,中國藥企多以「引進來」為主,向跨國藥企購買藥品或技術;如今,中國藥企正加速「走出去」,積極佈局國際市場。
中國創新藥,正在為全世界提供更多、更優質的治療方案。
在這股浪潮之中,一款針對皮膚疾病的中國創新藥,正在改寫數億患者的治療困境。
特應性皮炎,俗稱「濕疹」,全球患者接近 4 億人,是皮膚病中發病率最高的疾病。
值得關注的是,全球約 10%–20% 的兒童患有濕疹。
數據顯示,我國 1 歲以內 嬰幼兒患病率約為 30%,1 歲至 7 歲 兒童患病率約為 13%。
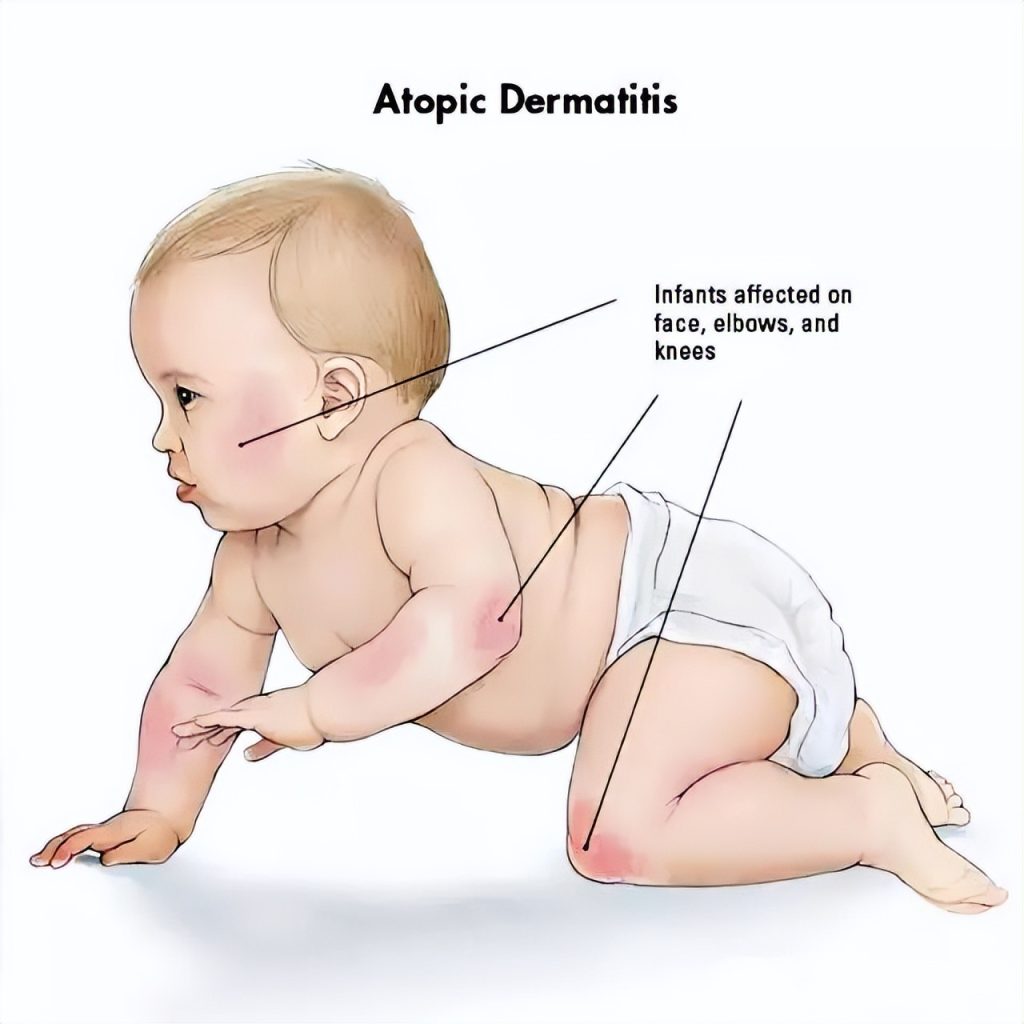
濕疹雖然不致命,卻因反覆且劇烈的瘙癢長期折磨患者,嚴重者甚至會影響 12 歲以下兒童 的生長發育,帶來失眠、外觀改變等問題,顯著降低生活品質。
長期以來,濕疹治療陷入「兩難困境」。
超過 90% 的患者採取外用藥治療:一類為類固醇(激素)藥物,起效迅速,但長期使用往往伴隨皮膚萎縮、色素沉著等風險;另一類為鈣調磷酸酶抑制劑,安全性較好,但起效較慢、療效相對有限。
兒童皮膚屏障脆弱、病情易反覆,加之家長對藥物副作用的顧慮,常導致用藥依從性不足,使治療陷入「不用藥孩子痛苦、用藥又心存顧慮」的惡性循環。
濕疹外用藥種類長期有限,難以滿足兒童患者的治療需求。
直到 2024 年,全球患者終於迎來了一款新藥。
2024 年 11 月 22 日,由上海澤德曼醫藥科技有限公司自主研發的 澤立美®(本維莫德乳膏) 獲得中國國家藥品監督管理局批准上市。

僅僅 20 天後,澤立美®(本維莫德乳膏) 再獲美國 FDA 批准,實現中美同步首發。
澤立美®(本維莫德乳膏)是我國自主研發、具備全新作用機制與靶點的創新藥物,亦是全球首個獲批准用於 2 歲以上兒童及成人濕疹(特應性皮炎) 治療的芳香烴受體(AhR)調節劑。
作為一款非激素類外用藥,澤立美®(本維莫德乳膏)的臨床效果顯示:患者用藥次日即可止癢;停藥 一年後,70% 的患者未出現復發。其全身暴露風險極低,主要不良反應僅為輕度毛囊炎。
首次在非激素類藥物中同時實現速效、高效與長效,這一卓越的治療表現,引起了**美國皮膚病學會(AAD)**的高度關注。
美國皮膚病學會(AAD)制定的臨床指南以嚴謹著稱,2014 年版指南發布後,歷經 9 年,方於 2023 年 完成修訂。
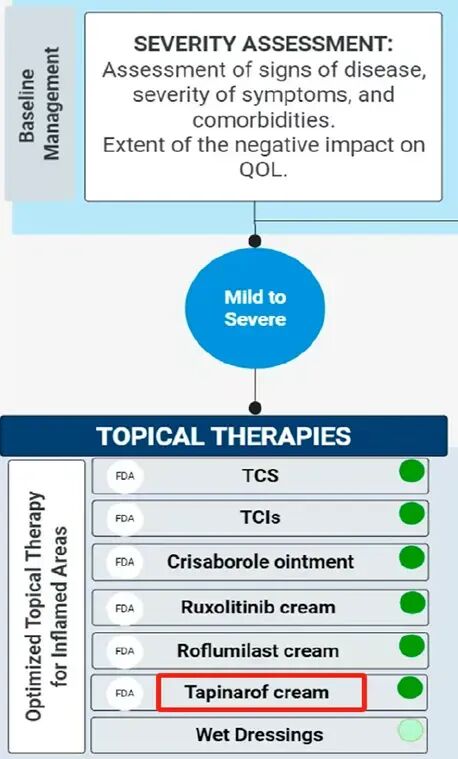
圖為 AAD 指南推薦的輕至重度特應性皮炎治療方案
Tapinarof 為本維莫德的海外名稱
在確認 澤立美®(本維莫德乳膏) 的臨床價值後,美國皮膚病學會(AAD)以史上最短修訂週期完成指南更新,並予以「強烈推薦」。
截至目前,澤立美®(本維莫德乳膏) 已陸續在中國、美國、日本、加拿大、德國及法國等多個國家獲批上市。
中國創新藥,正為全世界數億患者帶來全新的療法與選擇。
30 年的長跑
創新藥的研發向來被稱為「九死一生的冒險」,難度高、風險大、週期長、專業性強。
一款創新藥從早期研發到最終上市,平均需 10–15 年,投入 20–30 億美元,且臨床階段的成功率不足 10%。
澤立美®(本維莫德乳膏) 的誕生,正是這場「冒險」中跨越近 30 年 的堅持與突破。
上世紀 90 年代,正在加拿大 西蒙菲莎大學 攻讀生物學博士的 陳庚輝,與團隊成員一道,從一種土壤線蟲的共生細菌代謝產物中,分離出一種 芪類小分子化合物。

這便是日後震動全球皮膚科領域的 本維莫德(英文名 Tapinarof)。
別看本維莫德的分子量僅有 254 Da,卻能精準調控芳香烴受體(AhR)。
芳香烴受體(AhR)是一種廣泛表達於皮膚角質形成細胞、免疫細胞及上皮細胞中的細胞內配體活化轉錄因子。
如果把人體的免疫系統比作一棟房子,芳香烴受體(AhR)就像能夠控制所有燈光的總感應器。
一旦被啟動,便會引發一系列免疫反應。
陳庚輝及其團隊成員敏銳地意識到,透過本維莫德激活並調控芳香烴受體這一「超級靶點」,有望對引發皮膚炎症的相關細胞產生調節作用,從而抑制炎症與氧化應激,並促進皮膚屏障功能修復。
更為難得的是,本維莫德還具備良好的皮膚滲透性。
基於其生物學特性,本維莫德非常適合製成外用藥,用於治療各類皮膚疾病。
1999 年,陳庚輝與同窗 李建雄 及其導師 韋伯斯特 在加拿大正式創立公司,取得本維莫德的專利批件,開啟了系統性的研發之路。
其後,陳庚輝回國發展,創立公司持續推動本維莫德的臨床前研究及後續臨床試驗。
2019 年 5 月,本維莫德乳膏 獲批上市,用於成人輕中度尋常型銀屑病的治療。
2021 年,陳庚輝在上海浦東新區創立 澤德曼醫藥,開啟「第三次創業」,同時啟動了本維莫德的「二次開發」。

這一次,陳庚輝希望以 本維莫德乳膏 為基礎,開發 芳香烴受體(AhR)調節劑,攻克 特應性皮炎(濕疹) 這一皮膚病第一大病種。
2024 年 11 月,澤立美®(本維莫德乳膏) 在中美實現「雙報雙批」,創下中國新藥出海的重要里程碑。
「高投入、高風險、高失敗率、長週期」的研發特性,決定了創新藥在早期往往定價較高。
然而,澤立美®(本維莫德乳膏) 堅持平價惠民策略,國內初始定價僅為美國價格的 1/10。
為進一步提升藥品可及性,澤德曼醫藥 持續優化生產效率、嚴控成本並升級管理體系,並於 2025 年 7 月 進一步 降價 60%。
同時,澤德曼醫藥亦主動參與醫保談判,並已通過國家醫保初審。
未來,隨著醫保落地等政策紅利逐步釋放,國人將能以更親民的價格,使用到與國際同質同效的頂尖創新藥。
同一分子,兩次世界級突破!
陳庚輝及其團隊 堅守創新 30 載,不僅實現了一款藥物的雙適應症成功,更為中國創新藥樹立了從首發創新到全球認同的標杆。
創新方法論
從實驗室中的化合物,到全球矚目的創新藥,澤立美 的創新之路,為中國新藥研發提供了一套可借鑑的「創新方法論」。
需求導向,是創新的「指南針」。
創新的核心,在於回應真實的臨床需求。
澤立美的成功,源於對兒童特應性皮炎治療困境的精準洞察。
「創新不能為了創新而硬去創新,必須先弄清楚真正的需求在哪裡。」
陳庚輝坦言,自己的孩子曾患有濕疹,他親眼目睹臨床上對於兒童特應性皮炎用藥的迫切需求。
這份源自親身經驗的共情與洞察,使他堅定了研發方向。
這也啟示中國藥企:創新應扎根臨床一線,以患者痛點為原點,讓真實需求成為研發的「第一驅動力」。
專利佈局,是創新的「防護盾」。
針對特應性皮炎這一全新適應症,澤立美 構建了從化合物核心專利到製劑工藝、製造流程、適應症拓展的全鏈條專利矩陣,形成嚴密的智慧財產權保護網。
這既確保創新成果得到有效保護,使企業具備持續投入研發的能力,最終惠及全球更多患者;
亦表明,在創新藥領域,專利佈局的深度與廣度,直接決定企業的核心競爭力。
澤立美®(本維莫德乳膏)
長期主義,是創新的「定星盤」。
從上世紀 90 年代 分離化合物,到 2024 年 澤立美上市,陳庚輝及其團隊的創新之路跨越了近 30 年。其間歷經資金短缺、團隊動盪,卻始終堅守核心技術研發。
這種「十年磨一劍」的定力,正是當下中國新藥研發最為迫切需要的品質。
創新藥研發從來沒有「捷徑」,唯有堅守初心、長期投入,方能孕育出經得起臨床與市場雙重檢驗的重磅成果。
生態體系,是創新的「加速器」。
本維莫德雖在加拿大被發現,卻在中國完成了從實驗室到臨床應用的完整轉化。
澤立美的成功,離不開中國生物醫藥產業生態的全方位支撐。
一個關鍵細節是:澤立美於 2023 年 12 月 在中國完成上市申請受理,2024 年 1 月 納入優先審評,並於 同年 11 月 獲批上市。
從臨床到上市,中國僅用 523 天,而美國耗時 1,198 天,中國速度快了一倍以上。
這背後,既是中國藥審改革釋放的政策紅利,也是成熟產業生態協同發力的結果。
以澤德曼醫藥所在的 浦東新區 為例,當地生物醫藥產業規模高達 4,100 億元,集聚 4,000 多家 生物醫藥企業,在研創新藥管線 718 條,約占全國 1/5、全球 6%;累計獲批的國產創新藥與創新三類醫療器械,分別占全國的 13% 與 11%。

位於浦東新區張江高科園區的上海臨床創新轉化研究院
從基礎研究、孵化轉化,到臨床試驗、審評審批,再到落地生產與推廣應用,浦東新區所構建的「全鏈條創新生態」,為澤立美的研發與上市提供了從人才、資金到技術、政策的全方位支撐。
澤立美的成功,既是澤德曼醫藥堅持需求導向、深耕核心技術的結果,更是中國生物醫藥產業生態日益完善、政策與市場協同發力的必然體現。
這不僅為中國新藥研發提供了極具價值的實踐範本,也預示著中國創新藥正從「單點突破」邁向「體系化崛起」的新階段。
持續湧現
澤立美的創新傳奇,是中國新藥崛起的生動縮影。
在 2015–2025 年 的十年間,中國在研藥物數量由 851 個 激增至 7,041 個,複合年增長率達 23.5%,為全球平均水準(6.9%)的 3.4 倍。
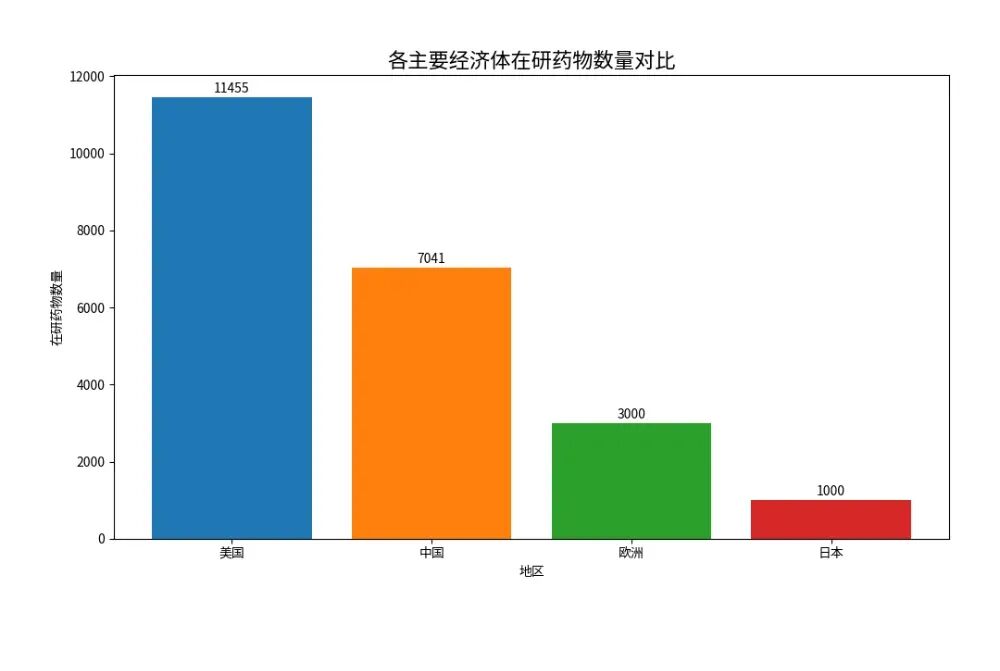
各主要經濟體在研藥物數量
更值得關注的是,我國 First-in-Class(全球首創) 藥物數量已由 2015 年的 9 個 激增至 2024 年的 120 個,全球占比由 9% 提升至 31.3%,位居全球第二,正快速逼近美國的領先地位。
正如本維莫德發明人、上海澤德曼醫藥科技有限公司董事長 陳庚輝博士 所言——過去是中國人等待西方新藥,現在是世界等待中國新藥。
這一判斷已被市場充分印證。2025 年上半年,中國創新藥 License-out(許可授權) 總金額已接近 660 億美元,超過去年全年總額。
輝瑞、葛蘭素史克、武田製藥 等國際製藥巨頭紛紛斥資重金布局中國創新藥,用真金白銀為中國原研實力投下信任票。
從「跟隨式創新」走向「源頭創新」的深刻轉型,正推動中國醫藥創新進入「質效雙升」的黃金時期,也正在重塑全球醫療產業的話語權格局。
展望未來,將有更多像 澤立美 這樣直擊臨床痛點、引領全球治療方向的創新藥物持續湧現。
全世界正在等待的中國新藥,正加速走來。

